ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲಿ ವಿದ್ಯುತ್ ಪ್ರವಾಹ
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲಿನ ವಿದ್ಯುತ್ ಪ್ರವಾಹವು ಯಾವಾಗಲೂ ವಸ್ತುವಿನ ವರ್ಗಾವಣೆಗೆ ಸಂಬಂಧಿಸಿದೆ. ಲೋಹಗಳು ಮತ್ತು ಅರೆವಾಹಕಗಳಲ್ಲಿ, ಉದಾಹರಣೆಗೆ, ಪ್ರಸ್ತುತವು ಅವುಗಳ ಮೂಲಕ ಹಾದುಹೋಗುವಾಗ ಮ್ಯಾಟರ್ ಅನ್ನು ವರ್ಗಾಯಿಸಲಾಗುವುದಿಲ್ಲ, ಏಕೆಂದರೆ ಈ ಮಾಧ್ಯಮಗಳಲ್ಲಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಮತ್ತು ರಂಧ್ರಗಳು ಪ್ರಸ್ತುತ ವಾಹಕಗಳಾಗಿವೆ, ಆದರೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲಿ ಅವುಗಳನ್ನು ವರ್ಗಾಯಿಸಲಾಗುತ್ತದೆ. ಏಕೆಂದರೆ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಲ್ಲಿ, ವಸ್ತುವಿನ ಧನಾತ್ಮಕ ಮತ್ತು ಋಣಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳು ಉಚಿತ ಚಾರ್ಜ್ಗಳ ವಾಹಕಗಳಾಗಿ ಕಾರ್ಯನಿರ್ವಹಿಸುತ್ತವೆ, ಎಲೆಕ್ಟ್ರಾನ್ಗಳು ಅಥವಾ ರಂಧ್ರಗಳಲ್ಲ.
ಅನೇಕ ಲೋಹಗಳ ಕರಗಿದ ಸಂಯುಕ್ತಗಳು, ಹಾಗೆಯೇ ಕೆಲವು ಘನವಸ್ತುಗಳು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯಗಳಿಗೆ ಸೇರಿವೆ. ಆದರೆ ತಂತ್ರಜ್ಞಾನದಲ್ಲಿ ವ್ಯಾಪಕವಾಗಿ ಬಳಸಲಾಗುವ ಈ ರೀತಿಯ ವಾಹಕಗಳ ಮುಖ್ಯ ಪ್ರತಿನಿಧಿಗಳು ಅಜೈವಿಕ ಆಮ್ಲಗಳು, ಬೇಸ್ಗಳು ಮತ್ತು ಲವಣಗಳ ಜಲೀಯ ದ್ರಾವಣಗಳಾಗಿವೆ.
ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯ ಮಾಧ್ಯಮದ ಮೂಲಕ ವಿದ್ಯುತ್ ಪ್ರವಾಹವು ಹಾದುಹೋದಾಗ ವಸ್ತುವು ವಿದ್ಯುದ್ವಾರಗಳ ಮೇಲೆ ಬಿಡುಗಡೆಯಾಗುತ್ತದೆ. ಈ ವಿದ್ಯಮಾನವನ್ನು ಕರೆಯಲಾಗುತ್ತದೆ ವಿದ್ಯುದ್ವಿಭಜನೆ… ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಮೂಲಕ ವಿದ್ಯುತ್ ಪ್ರವಾಹವು ಹಾದುಹೋದಾಗ, ವಸ್ತುವಿನ ಧನಾತ್ಮಕ ಮತ್ತು ಋಣಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳು ಏಕಕಾಲದಲ್ಲಿ ವಿರುದ್ಧ ದಿಕ್ಕುಗಳಲ್ಲಿ ಚಲಿಸುತ್ತವೆ.
ಋಣಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳು (ಅಯಾನುಗಳು) ಪ್ರಸ್ತುತ ಮೂಲದ (ಆನೋಡ್) ಧನಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರಕ್ಕೆ ಧಾವಿಸುತ್ತವೆ, ಮತ್ತು ಧನಾತ್ಮಕ ಆವೇಶದ ಅಯಾನುಗಳು (ಕ್ಯಾಥೋಡ್) ಅದರ ಋಣಾತ್ಮಕ ಧ್ರುವಕ್ಕೆ (ಕ್ಯಾಥೋಡ್).
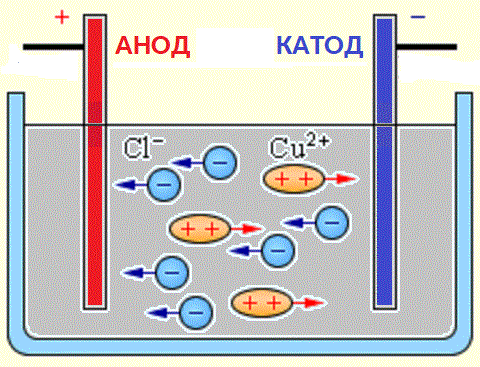
ಆಮ್ಲಗಳು, ಬೇಸ್ಗಳು ಮತ್ತು ಲವಣಗಳ ಜಲೀಯ ದ್ರಾವಣಗಳಲ್ಲಿ ಅಯಾನುಗಳ ಮೂಲಗಳು ತಟಸ್ಥ ಅಣುಗಳಾಗಿವೆ, ಅವುಗಳಲ್ಲಿ ಕೆಲವು ಅನ್ವಯಿಕ ವಿದ್ಯುತ್ ಬಲದ ಕ್ರಿಯೆಯ ಅಡಿಯಲ್ಲಿ ವಿಭಜನೆಯಾಗುತ್ತವೆ. ತಟಸ್ಥ ಅಣುಗಳನ್ನು ವಿಭಜಿಸುವ ಈ ವಿದ್ಯಮಾನವನ್ನು ಎಲೆಕ್ಟ್ರೋಲೈಟಿಕ್ ಡಿಸೋಸಿಯೇಷನ್ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ತಾಮ್ರದ ಕ್ಲೋರೈಡ್ CuCl2 ಕ್ಲೋರೈಡ್ ಅಯಾನುಗಳು (ಋಣಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ಡ್) ಮತ್ತು ತಾಮ್ರ (ಧನಾತ್ಮಕವಾಗಿ ಚಾರ್ಜ್ಡ್) ಆಗಿ ಜಲೀಯ ದ್ರಾವಣದಲ್ಲಿ ವಿಘಟನೆಯ ಮೇಲೆ ಕೊಳೆಯುತ್ತದೆ.
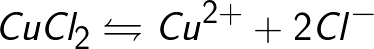
ವಿದ್ಯುದ್ವಾರಗಳನ್ನು ಪ್ರಸ್ತುತ ಮೂಲಕ್ಕೆ ಸಂಪರ್ಕಿಸಿದಾಗ, ಕ್ಲೋರಿನ್ ಅಯಾನುಗಳು ಆನೋಡ್ (ಧನಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರ) ಮತ್ತು ತಾಮ್ರದ ಕ್ಯಾಟಯಾನುಗಳಿಗೆ ಕ್ಯಾಥೋಡ್ (ಋಣಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರ) ಗೆ ಚಲಿಸುವುದರಿಂದ, ವಿದ್ಯುತ್ ಕ್ಷೇತ್ರವು ದ್ರಾವಣದಲ್ಲಿ ಅಥವಾ ಕರಗಿದ ಅಯಾನುಗಳ ಮೇಲೆ ಕಾರ್ಯನಿರ್ವಹಿಸಲು ಪ್ರಾರಂಭಿಸುತ್ತದೆ.
ಋಣಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರವನ್ನು ತಲುಪಿದಾಗ, ಧನಾತ್ಮಕ ಆವೇಶದ ತಾಮ್ರದ ಅಯಾನುಗಳು ಕ್ಯಾಥೋಡ್ನಲ್ಲಿರುವ ಹೆಚ್ಚುವರಿ ಎಲೆಕ್ಟ್ರಾನ್ಗಳಿಂದ ತಟಸ್ಥಗೊಳ್ಳುತ್ತವೆ ಮತ್ತು ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ಠೇವಣಿಯಾಗುವ ತಟಸ್ಥ ಪರಮಾಣುಗಳಾಗಿ ಮಾರ್ಪಡುತ್ತವೆ. ಧನಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರವನ್ನು ತಲುಪಿದಾಗ, ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ಡ್ ಕ್ಲೋರಿನ್ ಅಯಾನುಗಳು ಆನೋಡ್ನಲ್ಲಿನ ಧನಾತ್ಮಕ ಚಾರ್ಜ್ನೊಂದಿಗೆ ಪರಸ್ಪರ ಕ್ರಿಯೆಯ ಸಮಯದಲ್ಲಿ ಪ್ರತಿ ಎಲೆಕ್ಟ್ರಾನ್ ಅನ್ನು ದಾನ ಮಾಡುತ್ತವೆ. ಈ ಸಂದರ್ಭದಲ್ಲಿ, ರೂಪುಗೊಂಡ ತಟಸ್ಥ ಕ್ಲೋರಿನ್ ಪರಮಾಣುಗಳು ಜೋಡಿಯಾಗಿ ಸೇರಿ Cl2 ಅಣುಗಳನ್ನು ರೂಪಿಸುತ್ತವೆ ಮತ್ತು ಕ್ಲೋರಿನ್ ಆನೋಡ್ನಲ್ಲಿ ಅನಿಲ ಗುಳ್ಳೆಗಳ ರೂಪದಲ್ಲಿ ಬಿಡುಗಡೆಯಾಗುತ್ತದೆ.
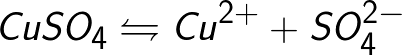
ಆಗಾಗ್ಗೆ, ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಪ್ರಕ್ರಿಯೆಯು ವಿಘಟನೆಯ ಉತ್ಪನ್ನಗಳ ಪರಸ್ಪರ ಕ್ರಿಯೆಯೊಂದಿಗೆ ಇರುತ್ತದೆ (ಇದನ್ನು ದ್ವಿತೀಯಕ ಪ್ರತಿಕ್ರಿಯೆಗಳು ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ), ವಿದ್ಯುದ್ವಾರಗಳ ಮೇಲೆ ಬಿಡುಗಡೆಯಾದ ವಿಭಜನೆಯ ಉತ್ಪನ್ನಗಳು ದ್ರಾವಕದೊಂದಿಗೆ ಅಥವಾ ನೇರವಾಗಿ ವಿದ್ಯುದ್ವಾರ ವಸ್ತುಗಳೊಂದಿಗೆ ಸಂವಹನ ನಡೆಸಿದಾಗ. ಉದಾಹರಣೆಗೆ, ತಾಮ್ರದ ಸಲ್ಫೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದ ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ತೆಗೆದುಕೊಳ್ಳಿ (ತಾಮ್ರದ ಸಲ್ಫೇಟ್ - CuSO4).ಈ ಉದಾಹರಣೆಯಲ್ಲಿ, ವಿದ್ಯುದ್ವಾರಗಳನ್ನು ತಾಮ್ರದಿಂದ ಮಾಡಲಾಗುವುದು.
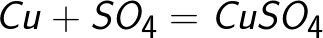
ತಾಮ್ರದ ಸಲ್ಫೇಟ್ ಅಣುವು ಧನಾತ್ಮಕ ಆವೇಶದ ತಾಮ್ರದ ಅಯಾನು Cu + ಮತ್ತು ಋಣಾತ್ಮಕ ಚಾರ್ಜ್ಡ್ ಸಲ್ಫೇಟ್ ಅಯಾನು SO4- ಅನ್ನು ರೂಪಿಸಲು ವಿಭಜನೆಯಾಗುತ್ತದೆ. ತಟಸ್ಥ ತಾಮ್ರದ ಪರಮಾಣುಗಳನ್ನು ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ಘನ ಠೇವಣಿಯಾಗಿ ಸಂಗ್ರಹಿಸಲಾಗುತ್ತದೆ. ಈ ರೀತಿಯಾಗಿ, ರಾಸಾಯನಿಕವಾಗಿ ಶುದ್ಧ ತಾಮ್ರವನ್ನು ಪಡೆಯಲಾಗುತ್ತದೆ.
ಸಲ್ಫೇಟ್ ಅಯಾನು ಧನಾತ್ಮಕ ವಿದ್ಯುದ್ವಾರಕ್ಕೆ ಎರಡು ಎಲೆಕ್ಟ್ರಾನ್ಗಳನ್ನು ದಾನ ಮಾಡುತ್ತದೆ ಮತ್ತು ತಟಸ್ಥ ರಾಡಿಕಲ್ SO4 ಆಗುತ್ತದೆ, ಇದು ತಕ್ಷಣವೇ ತಾಮ್ರದ ಆನೋಡ್ನೊಂದಿಗೆ ಪ್ರತಿಕ್ರಿಯಿಸುತ್ತದೆ (ಸೆಕೆಂಡರಿ ಆನೋಡ್ ಪ್ರತಿಕ್ರಿಯೆ). ಆನೋಡ್ನಲ್ಲಿನ ಪ್ರತಿಕ್ರಿಯೆ ಉತ್ಪನ್ನವು ತಾಮ್ರದ ಸಲ್ಫೇಟ್ ಆಗಿದೆ, ಇದು ದ್ರಾವಣಕ್ಕೆ ಹೋಗುತ್ತದೆ.
ತಾಮ್ರದ ಸಲ್ಫೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದ ಮೂಲಕ ವಿದ್ಯುತ್ ಪ್ರವಾಹವು ಹಾದುಹೋದಾಗ, ತಾಮ್ರದ ಆನೋಡ್ ಕ್ರಮೇಣ ಕರಗುತ್ತದೆ ಮತ್ತು ತಾಮ್ರವು ಕ್ಯಾಥೋಡ್ನಲ್ಲಿ ಅವಕ್ಷೇಪಿಸುತ್ತದೆ.ಈ ಸಂದರ್ಭದಲ್ಲಿ, ತಾಮ್ರದ ಸಲ್ಫೇಟ್ನ ಜಲೀಯ ದ್ರಾವಣದ ಸಾಂದ್ರತೆಯು ಬದಲಾಗುವುದಿಲ್ಲ.
1833 ರಲ್ಲಿ, ಇಂಗ್ಲಿಷ್ ಭೌತಶಾಸ್ತ್ರಜ್ಞ ಮೈಕೆಲ್ ಫ್ಯಾರಡೆ, ಪ್ರಾಯೋಗಿಕ ಕೆಲಸದ ಸಂದರ್ಭದಲ್ಲಿ, ವಿದ್ಯುದ್ವಿಭಜನೆಯ ನಿಯಮವನ್ನು ಸ್ಥಾಪಿಸಿದರು, ಅದನ್ನು ಈಗ ಅವರ ಹೆಸರಿಡಲಾಗಿದೆ.
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಸಮಯದಲ್ಲಿ ವಿದ್ಯುದ್ವಾರಗಳ ಮೇಲೆ ಬಿಡುಗಡೆಯಾಗುವ ಪ್ರಾಥಮಿಕ ಉತ್ಪನ್ನಗಳ ಪ್ರಮಾಣವನ್ನು ನಿರ್ಧರಿಸಲು ಫ್ಯಾರಡೆ ಕಾನೂನು ನಿಮಗೆ ಅನುಮತಿಸುತ್ತದೆ. ಕಾನೂನು ಈ ಕೆಳಗಿನವುಗಳನ್ನು ಹೇಳುತ್ತದೆ: "ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಸಮಯದಲ್ಲಿ ವಿದ್ಯುದ್ವಾರದ ಮೇಲೆ ಬಿಡುಗಡೆಯಾಗುವ ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿ m ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಮೂಲಕ ಹಾದುಹೋಗುವ ಚಾರ್ಜ್ Q ಗೆ ನೇರವಾಗಿ ಅನುಪಾತದಲ್ಲಿರುತ್ತದೆ."
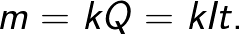
ಈ ಸೂತ್ರದಲ್ಲಿ ಅನುಪಾತದ ಅಂಶ k ಅನ್ನು ಎಲೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸಮಾನ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಸಮಯದಲ್ಲಿ ವಿದ್ಯುದ್ವಾರದ ಮೇಲೆ ಬಿಡುಗಡೆಯಾಗುವ ವಸ್ತುವಿನ ದ್ರವ್ಯರಾಶಿಯು ಈ ವಿದ್ಯುದ್ವಾರಕ್ಕೆ ಬಂದ ಎಲ್ಲಾ ಅಯಾನುಗಳ ಒಟ್ಟು ದ್ರವ್ಯರಾಶಿಗೆ ಸಮಾನವಾಗಿರುತ್ತದೆ:
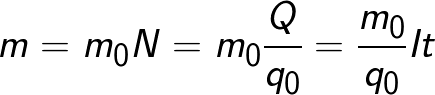
ಸೂತ್ರವು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಮೂಲಕ ಹಾದುಹೋಗುವ ಚಾರ್ಜ್ q0 ಮತ್ತು ಅಯಾನಿನ ದ್ರವ್ಯರಾಶಿ m0 ಅನ್ನು ಒಳಗೊಂಡಿರುತ್ತದೆ, ಹಾಗೆಯೇ ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಮೂಲಕ ಹಾದುಹೋಗುವ ಚಾರ್ಜ್ Q. N ಎಂಬುದು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಮೂಲಕ ಚಾರ್ಜ್ Q ಹಾದುಹೋದಾಗ ವಿದ್ಯುದ್ವಾರಕ್ಕೆ ಬಂದ ಅಯಾನುಗಳ ಸಂಖ್ಯೆ.ಆದ್ದರಿಂದ, ಅಯಾನು m0 ದ್ರವ್ಯರಾಶಿಯ ಅನುಪಾತವನ್ನು ಅದರ ಚಾರ್ಜ್ q0 ಗೆ k ನ ಎಲೆಕ್ಟ್ರೋಕೆಮಿಕಲ್ ಸಮಾನ ಎಂದು ಕರೆಯಲಾಗುತ್ತದೆ.
ಅಯಾನಿನ ಚಾರ್ಜ್ ಸಂಖ್ಯಾತ್ಮಕವಾಗಿ ವಸ್ತುವಿನ ವೇಲೆನ್ಸಿ ಮತ್ತು ಪ್ರಾಥಮಿಕ ಚಾರ್ಜ್ನ ಉತ್ಪನ್ನಕ್ಕೆ ಸಮಾನವಾಗಿರುವುದರಿಂದ, ರಾಸಾಯನಿಕ ಸಮಾನತೆಯನ್ನು ಈ ಕೆಳಗಿನ ರೂಪದಲ್ಲಿ ಪ್ರತಿನಿಧಿಸಬಹುದು:
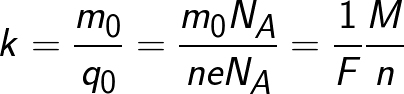
ಎಲ್ಲಿ: Na ಎಂಬುದು ಅವೊಗಾಡ್ರೊ ಸ್ಥಿರಾಂಕ, M ಎಂಬುದು ವಸ್ತುವಿನ ಮೋಲಾರ್ ದ್ರವ್ಯರಾಶಿ, F ಎಂಬುದು ಫ್ಯಾರಡೆಯ ಸ್ಥಿರವಾಗಿರುತ್ತದೆ.
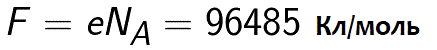
ವಾಸ್ತವವಾಗಿ, ಫ್ಯಾರಡೆ ಸ್ಥಿರಾಂಕವನ್ನು ವಿದ್ಯುದ್ವಿಚ್ಛೇದ್ಯದ ಮೂಲಕ ಹಾದು ಹೋಗಬೇಕಾದ ಚಾರ್ಜ್ ಪ್ರಮಾಣ ಎಂದು ವ್ಯಾಖ್ಯಾನಿಸಬಹುದು, ಇದು ಎಲೆಕ್ಟ್ರೋಡ್ನಲ್ಲಿನ ಒಂದು ಮೋಲ್ ಮೋನೋವೆಲೆಂಟ್ ವಸ್ತುವನ್ನು ಬಿಡುಗಡೆ ಮಾಡುತ್ತದೆ. ಫ್ಯಾರಡೆಯ ವಿದ್ಯುದ್ವಿಭಜನೆಯ ನಿಯಮವು ನಂತರ ರೂಪವನ್ನು ಪಡೆಯುತ್ತದೆ:
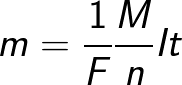
ವಿದ್ಯುದ್ವಿಭಜನೆಯ ವಿದ್ಯಮಾನವನ್ನು ಆಧುನಿಕ ಉತ್ಪಾದನೆಯಲ್ಲಿ ವ್ಯಾಪಕವಾಗಿ ಬಳಸಲಾಗುತ್ತದೆ. ಉದಾಹರಣೆಗೆ, ಅಲ್ಯೂಮಿನಿಯಂ, ತಾಮ್ರ, ಹೈಡ್ರೋಜನ್, ಮ್ಯಾಂಗನೀಸ್ ಡೈಆಕ್ಸೈಡ್ ಮತ್ತು ಹೈಡ್ರೋಜನ್ ಪೆರಾಕ್ಸೈಡ್ ಅನ್ನು ವಿದ್ಯುದ್ವಿಭಜನೆಯಿಂದ ಕೈಗಾರಿಕಾವಾಗಿ ಉತ್ಪಾದಿಸಲಾಗುತ್ತದೆ. ಅನೇಕ ಲೋಹಗಳನ್ನು ಅದಿರುಗಳಿಂದ ಹೊರತೆಗೆಯಲಾಗುತ್ತದೆ ಮತ್ತು ವಿದ್ಯುದ್ವಿಭಜನೆಯ ಮೂಲಕ ಸಂಸ್ಕರಿಸಲಾಗುತ್ತದೆ (ಎಲೆಕ್ಟ್ರೋಫೈನಿಂಗ್ ಮತ್ತು ಎಲೆಕ್ಟ್ರೋಎಕ್ಟ್ರಾಕ್ಷನ್).
ಅಲ್ಲದೆ, ವಿದ್ಯುದ್ವಿಭಜನೆಗೆ ಧನ್ಯವಾದಗಳು, ರಾಸಾಯನಿಕ ಪ್ರಸ್ತುತ ಮೂಲಗಳು… ವಿದ್ಯುದ್ವಿಭಜನೆಯನ್ನು ತ್ಯಾಜ್ಯನೀರಿನ ಸಂಸ್ಕರಣೆಯಲ್ಲಿ ಬಳಸಲಾಗುತ್ತದೆ (ವಿದ್ಯುತ್ ಹೊರತೆಗೆಯುವಿಕೆ, ಎಲೆಕ್ಟ್ರೋಕೋಗ್ಯುಲೇಷನ್, ಎಲೆಕ್ಟ್ರೋಫ್ಲೋಟೇಶನ್). ಅನೇಕ ವಸ್ತುಗಳನ್ನು (ಲೋಹಗಳು, ಹೈಡ್ರೋಜನ್, ಕ್ಲೋರಿನ್, ಇತ್ಯಾದಿ) ವಿದ್ಯುದ್ವಿಭಜನೆಯಿಂದ ಪಡೆಯಲಾಗುತ್ತದೆ ಎಲೆಕ್ಟ್ರೋಪ್ಲೇಟಿಂಗ್ ಮತ್ತು ಎಲೆಕ್ಟ್ರೋಪ್ಲೇಟಿಂಗ್ಗಾಗಿ.
ಸಹ ನೋಡಿ:ನೀರಿನ ವಿದ್ಯುದ್ವಿಭಜನೆಯಿಂದ ಹೈಡ್ರೋಜನ್ ಉತ್ಪಾದನೆ - ತಂತ್ರಜ್ಞಾನ ಮತ್ತು ಉಪಕರಣಗಳು

